Virus di Epstein-Barr: il virus nascosto che può causare malattie croniche
🥼 Virus di Epstein-Barr. Lo conosci? Un virus silenzioso che può causare più di una semplice mononucleosi...

Introduzione
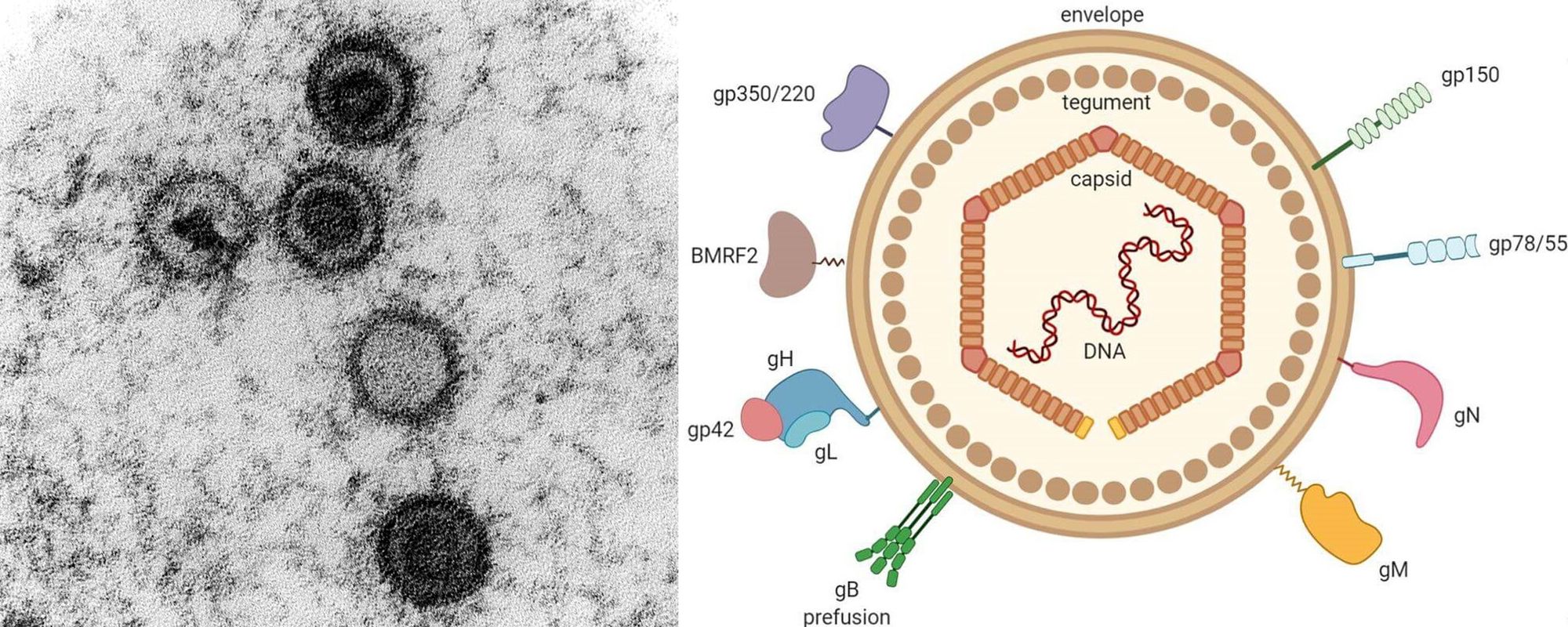
Il virus di Epstein-Barr (EBV), conosciuto anche come herpesvirus di tipo 4 (human herpesvirus 4, HHV-4) è un virus a DNA, di forma sferoidale, formato da un capside icosaedrico di 100-110 nm di diametro, e rivestito dal pericapside (o envelope), una membrana di lipoproteine che costituisce lo strato più esterno (Fig. 1). Dal punto di vista tassonomico, l’EBV rientra nella famiglia degli Herpesvirus e nella sottofamiglia dei Gamma herpesvirus, il cui nome indica gli herpesvirus che si replicano lentamente e possono immortalizzare le cellule con conseguente trasformazione tumorale.
Il primo isolamento dell’EBV avvenne a Londra nel 1964 da parte di due virologi inglesi, Anthony Epstein e Yvonne Barr, i quali analizzarono delle cellule in coltura provenienti dall’Uganda, che erano state prelevate da pazienti affetti da un linfoma che poi sarà denominato linfoma di Burkitt, dal nome del patologo e chirurgo britannico Dennis Parsons Burkitt. Costui aveva identificato e descritto tale patologia, diffusa particolarmente nell’Africa sub-sahariana, e aveva effettuato i prelievi.
Mediante osservazione al microscopio elettronico delle cellule in coltura, Epstein e Barr distinsero un nuovo herpesvirus, che prese il nome di virus di Epstein-Barr.
Filogenesi
Dominio Duplodnaviria
Regno Heunggongvirae
Phylum Peploviricota
Classe Herviviricetes
Ordine Herpesvirales
Famiglia Herpesviridae
Sottofamiglia Gammaherpesvirinae
Genere Lymphocryptovirus
Specie Human herpesvirus 4
Genoma
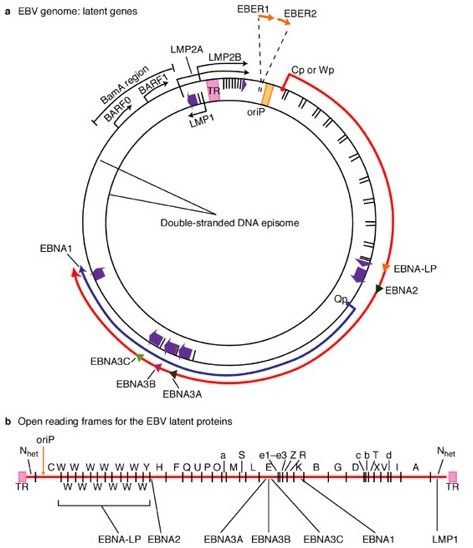
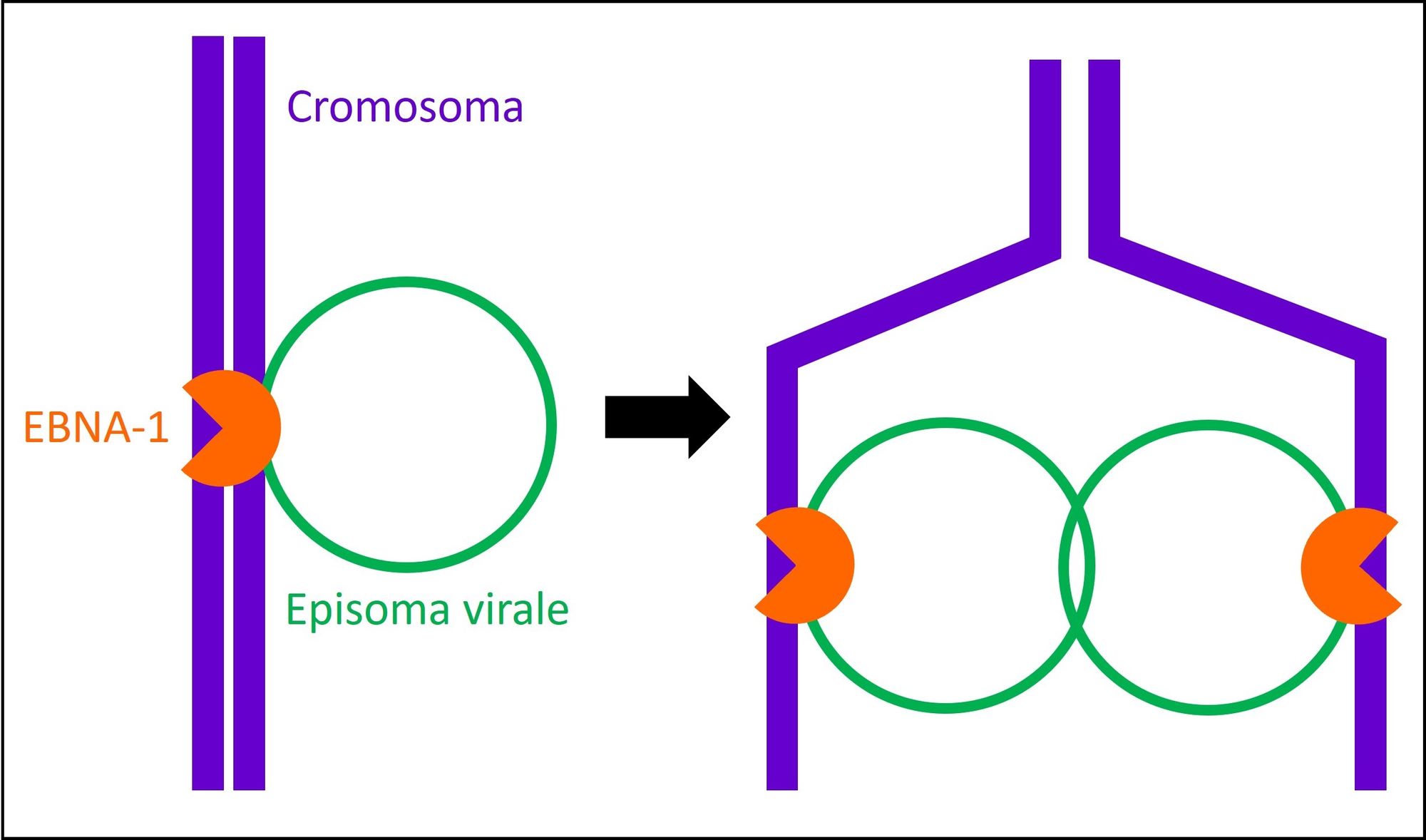
Al livello genetico, l’HHV-4 presenta un genoma lineare e a doppio filamento di DNA che codifica per più di 85 geni ed è diviso in due domini di sequenza unica, lungo e corto. La maggioranza delle proteine codificate dai geni di EBV ha la funzione di mantenere la replicazione virale e di costruire i compartimenti strutturali del virus, tra cui le proteine che compongono il capside. In aggiunta a ciò, possiede diversi geni latenti, ovvero che non vengono espressi quando il virus è in attiva replicazione (ciclo litico), bensì nel momento in cui rimane nelle cellule in maniera latente senza replicarsi. Tra questi geni abbiamo sei proteine nucleari (EBNA-1, EBNA-2, EBNA-3A, EBNA-3B, EBNA-3C e EBNA-LP) e tre proteine di membrana (LMP-1, LMP-2A e LMP-2B) (Fig. 2). Focalizzandoci su EBNA-1 e LMP-1, la prima è l’unica proteina latente espressa in maniera costitutiva, e permette l’adesione dell’episoma virale ai cromosomi della cellula ospite, garantendo la segregazione nelle cellule figlie degli episomi replicati durante la divisione cellulare (Fig. 3). Il termine “episoma” indica il genoma virale che si trova nel nucleo delle cellule, in forma circolare, e che non si integra nel genoma cellulare. La seconda raffigura la proteina oncogena, ovvero che promuove la trasformazione cancerogena delle cellule infette, mediante un meccanismo di cui parleremo più avanti. Data questa abilità, l’EBV è incluso nella cerchia dei virus oncogeni insieme all’HPV (Papillomavirus umano), l’HBV (virus dell’epatite B), l’HCV (virus dell’epatite C), il KSHV (virus del sarcoma di Kaposi) e l’HTLV-1 e 2 (virus della leucemia umana a cellule T).
Trasmissione e ciclo biologico
L’HHV-4 si trasmette prevalentemente attraverso la saliva (direttamente o indirettamente), e al giorno d’oggi raffigura un virus abbastanza ubiquitario, presente in maniera asintomatica nel 90-95% della popolazione mondiale. Nei paesi in via di sviluppo il primo contatto con il virus si verifica di solito nell’infanzia, mentre nei paesi sviluppati è più comune durante l’adolescenza e l’età adulta. In gran parte dei casi l’infezione passa inosservata e non dà alcun segno clinico, mentre in altre circostanze può provocare la mononucleosi (la cosiddetta “malattia del bacio”), che colpisce principalmente adolescenti e adulti.
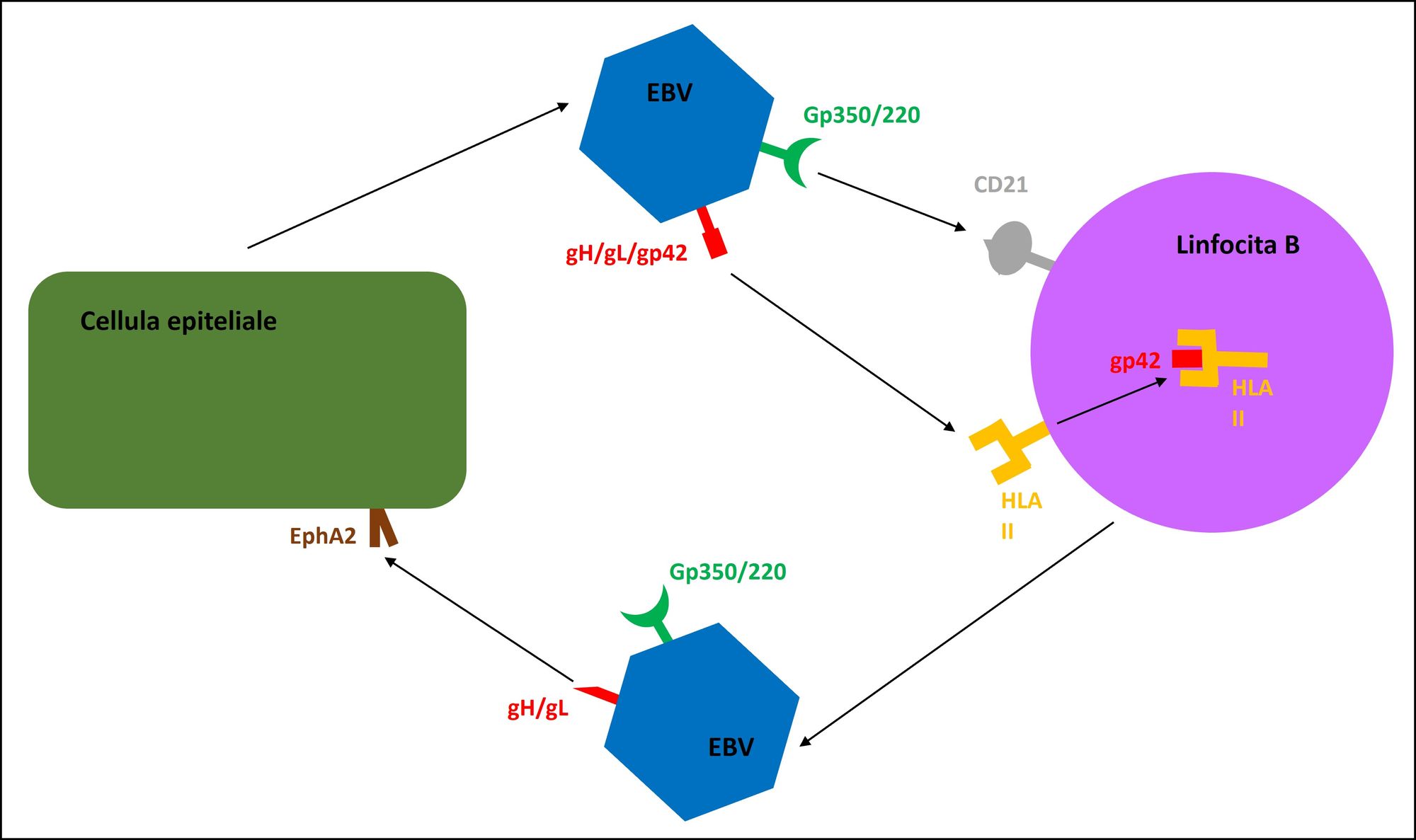
Nel momento in cui il virus entra in un individuo, in genere attraverso la cavità orale, infetta i linfociti B (cellule immunitarie deputate alla produzione di anticorpi) e le cellule epiteliali che ricoprono le tonsille (cheratinociti), dove inizia un ciclo litico; quello effettuato nei cheratinociti ricorda quello del Papillomavirus.
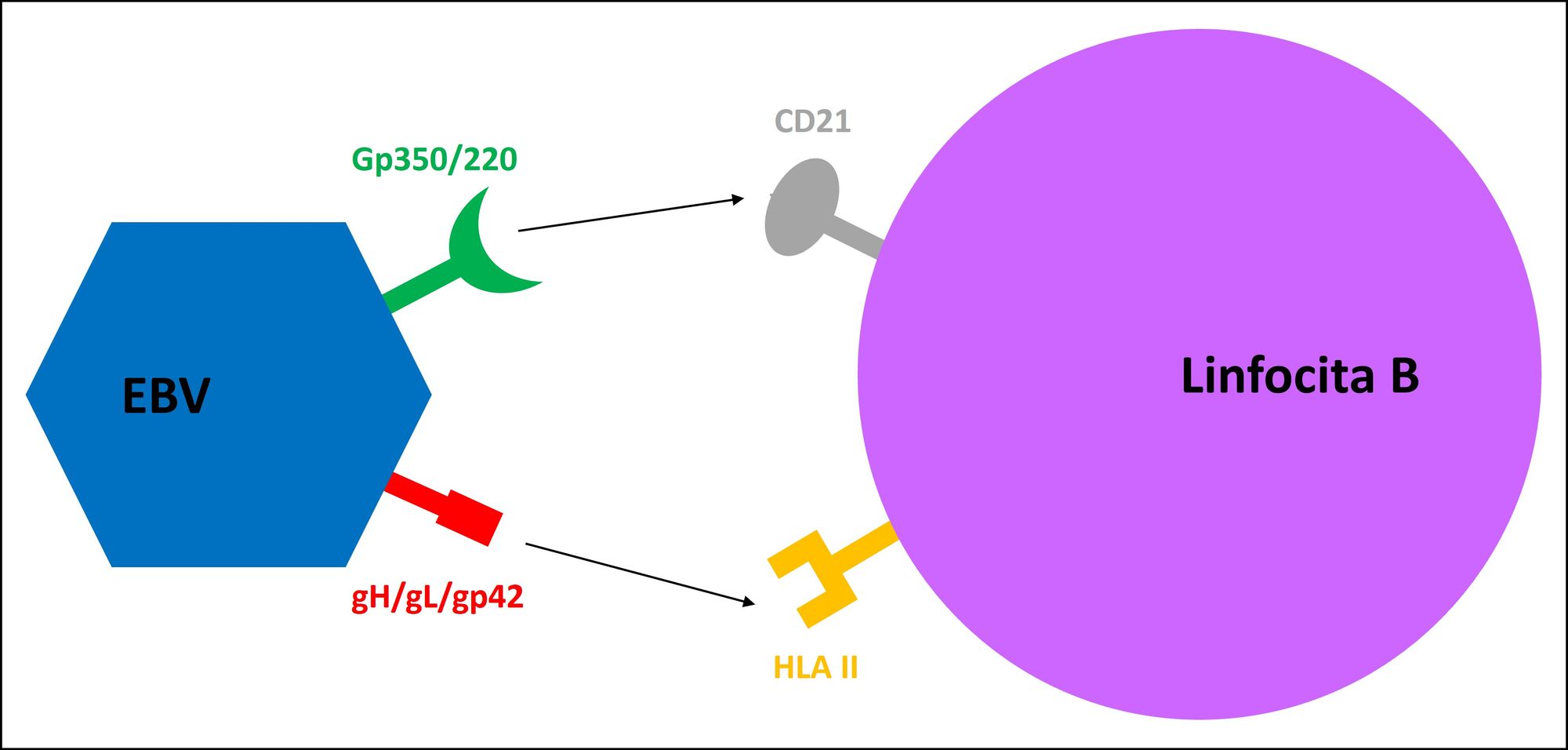
Il tropismo di EBV è raffigurato dai linfociti B, che esprimono due recettori, il CD21 (o CR2) e le HLA II (molecole del complesso maggiore di istocompatibilità di tipo II), con i quali il virus interagisce mediante due antigeni del pericapside, cioè gp350/220 e gH/gL/gp42 rispettivamente (Fig. 4). A questo punto ci si può porre la seguente domanda: considerando che le cellule epiteliali non esprimono i due recettori dei linfociti B, come fa il virus a infettarle? La risposta sta nella capacità dell’EBV di effettuare un cambiamento recettoriale in seguito alla penetrazione e alla replicazione all’interno dei linfociti: l’antigene gH/gL/gp42 si modifica in gH/gL, dal momento che gp42 si lega alle HLA II per essere presentato ai linfociti T (un altro tipo di cellule immunitarie). La rimozione di gb42 consente ai nuovi virioni di interagire con un recettore dei cheratinociti, ossia EphA2 (recettore 2 dell’efrina A). Dipoi i virioni emessi dalle cellule epiteliali riacquistano la particella gp42 e possono infettare altri linfociti, dunque ricominciare il ciclo. (Fig. 5).
Nel momento in cui l’EBV parassita i linfociti B, inizia la fase di attiva replicazione, che precede quella di latenza, e produce nuovi virus; al contempo i linfociti si attivano, diventano linfoblasti, migrano ai linfonodi ed espongono gli antigeni virali ai linfociti T, che eliminano le cellule appena infettate, provvedono a controllare l’infezione e inducono i linfociti B attivati a differenziarsi in plasmacellule, che rilasciano anticorpi, e in linfociti della memoria (le cellule che permangono dopo un’infezione e proteggono in caso di un secondo contatto con lo stesso agente patogeno). Quando si passa dall’infezione primaria a quella latente, il virus si mantiene silente nei linfociti della memoria rimanenti che circolano nel sangue, e non è individuabile dal sistema immunitario.
Patogenesi
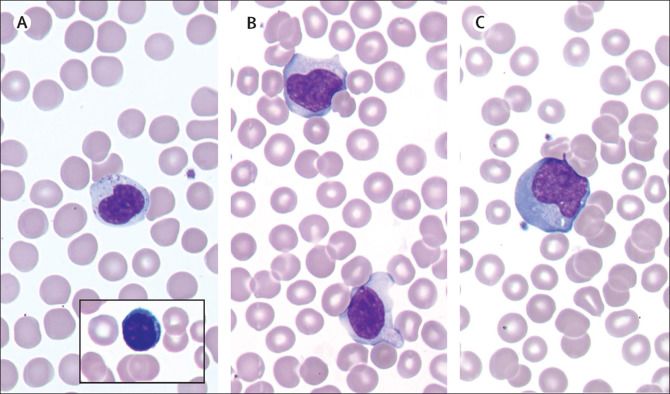
L’infezione da HHV-4 può passare inosservata oppure determinare l’insorgenza di varie patologie, di cui la più diffusa e nota è la mononucleosi infettiva, caratterizzata da sintomi aspecifici come febbre, linfoadenopatia (ingrossamento dei linfonodi), debolezza, faringite e, nel 50% dei casi, splenomegalia (accrescimento della milza). All’esame emocromocitometrico si evidenzia un’alta concentrazione di linfociti, mentre l’esame microscopico mette in risalto le cellule di Downey (o virociti), ovvero linfociti di dimensioni e forma instabili, con il nucleo lobulato o reniforme, e il citoplasma basofilo, che aderiscono agli eritrociti vicini (Fig. 6). I virociti sono i primi linfociti T che agiscono per eradicare il virus; la parola “mononucleosi” è data proprio dalla grossa quantità di queste cellule che, proliferando, arrivano a costituire fino all’80% delle cellule del sangue.
Di solito la malattia è autolimitante e guarisce senza alcun trattamento dopo circa due settimane. Raramente insorgono complicanze come convulsioni, danni neurologici, encefalite, meningite, rottura della milza e blocco delle vie aeree a causa dei linfonodi gonfi.
Altre malattie sono quelle tumorali, tra cui il carcinoma nasofaringeo, il linfoma di Burkitt e il linfoma di Hodgkin. Il primo, che ha un’incidenza maggiore in Cina e in Turchia, colpisce l’epitelio che riveste la mucosa nasofaringea; l’espansione della neoplasia conduce all’invasione di diverse zone limitrofe, come l’interno o l’esterno del nasofaringe, la base del cranio e del palato, la cavità nasale e l’orofaringe, e metastatizza soprattutto ai linfonodi cervicali. I sintomi possono essere linfoadenopatia cervicale, ostruzione del naso, emorragia e “voce nasale”.
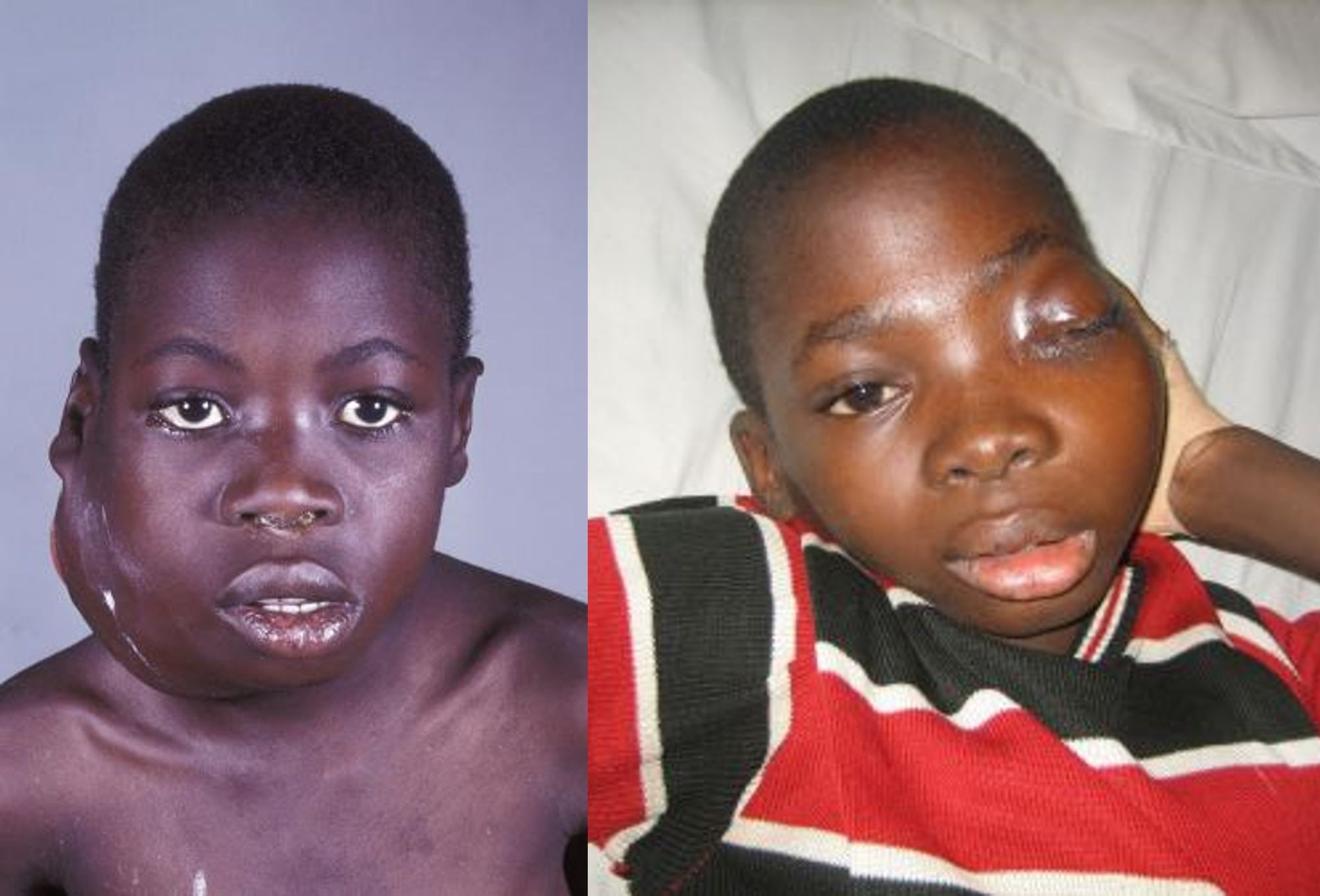
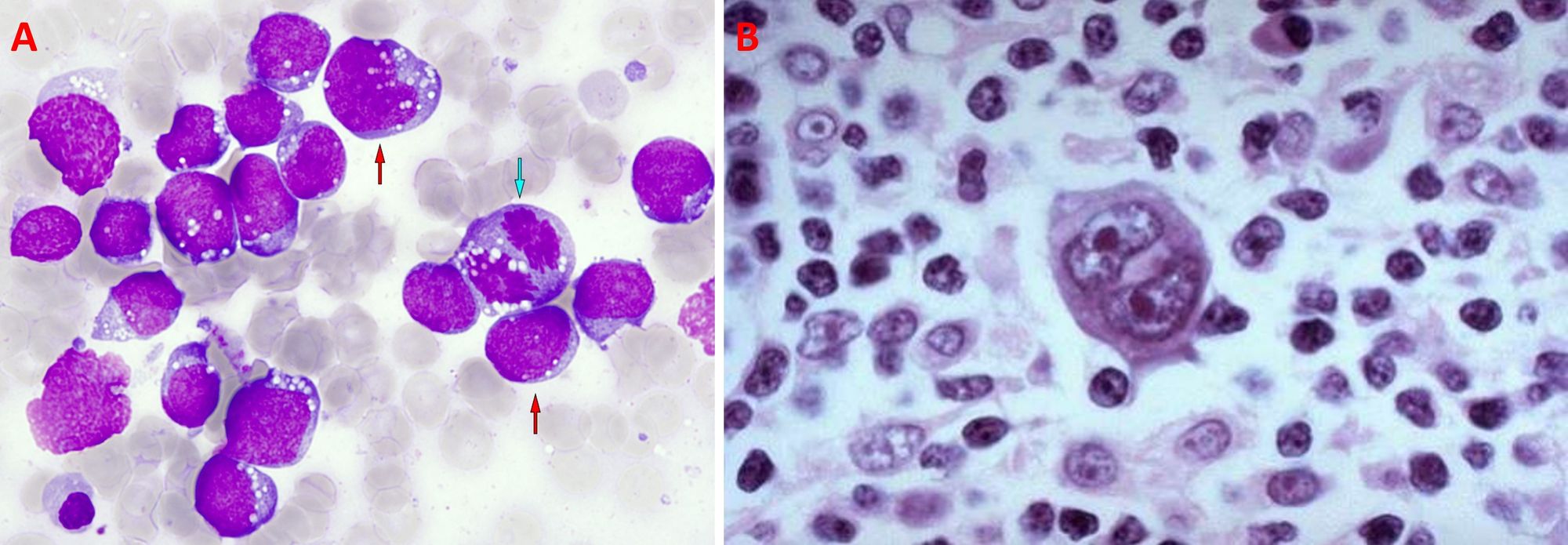
Passando al secondo, c’è da dire che è endemico specialmente tra i bambini dell’Africa equatoriale e della Nuova Guinea, dove ha una correlazione con la malaria. Questo tumore, che è altamente aggressivo, ha come protagonisti i linfociti B, in particolare quelli localizzati nei linfonodi mascellari, che si moltiplicano velocemente provocando un incremento del volume della mascella e delle ossa facciali (Fig. 7). Le cellule tumorali mostrano le seguenti caratteristiche: nucleo rotondo, nucleoli multipli, citoplasma basofilo contenente vacuoli (Fig. 8A); di rado si localizzano nel midollo o entrano nel circolo ematico.
Per quanto concerne l’ultimo, anch’esso origina dai linfociti B causando un turgore dei linfonodi, specie quelli della regione cervicale. Si propaga in senso centripeto e in maniera contigua, cioè dal primo linfonodo coinvolto passa a quelli adiacenti seguendo il percorso dei vasi linfatici; al livello istologico contiene poche cellule tumorali, immerse in una quantità cospicua di cellule infiammatorie, e delle cellule giganti chiamate cellule di Reed-Sternberg, che appaiono con un singolo nucleo plurilobato o con nuclei multipli, molteplici nucleoli e inclusioni nucleari eosinofile (Fig. 8B). I sintomi sono febbre, stanchezza, sudorazione notturna, calo ponderale e prurito.
Un’ulteriore patologia dovuta all’EBV sono i disordini linfoproliferativi post-trapianto, che sono distinti da una proliferazione anormale dei linfociti B, e possono insorgere in seguito a trapianto di cellule staminali ematopoietiche o di organi solidi. Il rischio è maggiore nel primo anno dopo il trapianto e la malattia spesso è fatale. I principali fattori che aumentano la probabilità di insorgenza sono la sieronegatività pre-trapianto e l’infezione primaria post-trapianto, la rimozione della milza prima del trapianto, l’età pediatrica, la co-infezione con il citomegalovirus, un’intensa terapia immunosoppressiva e la positività del donatore all’EBV.
Uno sguardo all’oncogenesi
L’HHV-4 promuove l’immortalizzazione delle cellule e la conseguente trasformazione cancerogena mediante la proteina di membrana LMP-1, che aumenta l’espressione delle molecole di adesione e dei geni che inibiscono l’apoptosi (morte cellulare programmata) (BCL-2), attiva le vie di segnalazione che favoriscono la proliferazione e la sopravvivenza cellulare (NF-kB, PI3K/Akt, MEK/ERK, JAK/STAT), abbassa l’espressione dei geni che controllano la divisione cellulare (p16, p27), sostiene l’angiogenesi (creazione di nuovi vasi sanguigni) e la metastatizzazione. Anche LMP-2A dà il suo contributo alla genesi dei tumori supportando la sopravvivenza cellulare e la latenza del virus. Due lavori del 1998, pubblicati su PNAS e Immunity, mostrano due modelli murini transgenici (geneticamente modificati) caratterizzati da linfociti B con un’espressione aumentata di LMP-1 e LMP-2A rispettivamente. I topi LMP-1 sviluppano il linfoma a cellule B, mentre nei topi LMP-2A la maturazione dei linfociti B è alterata e ciò permette l’entrata e la persistenza di cellule immature nel sangue periferico.
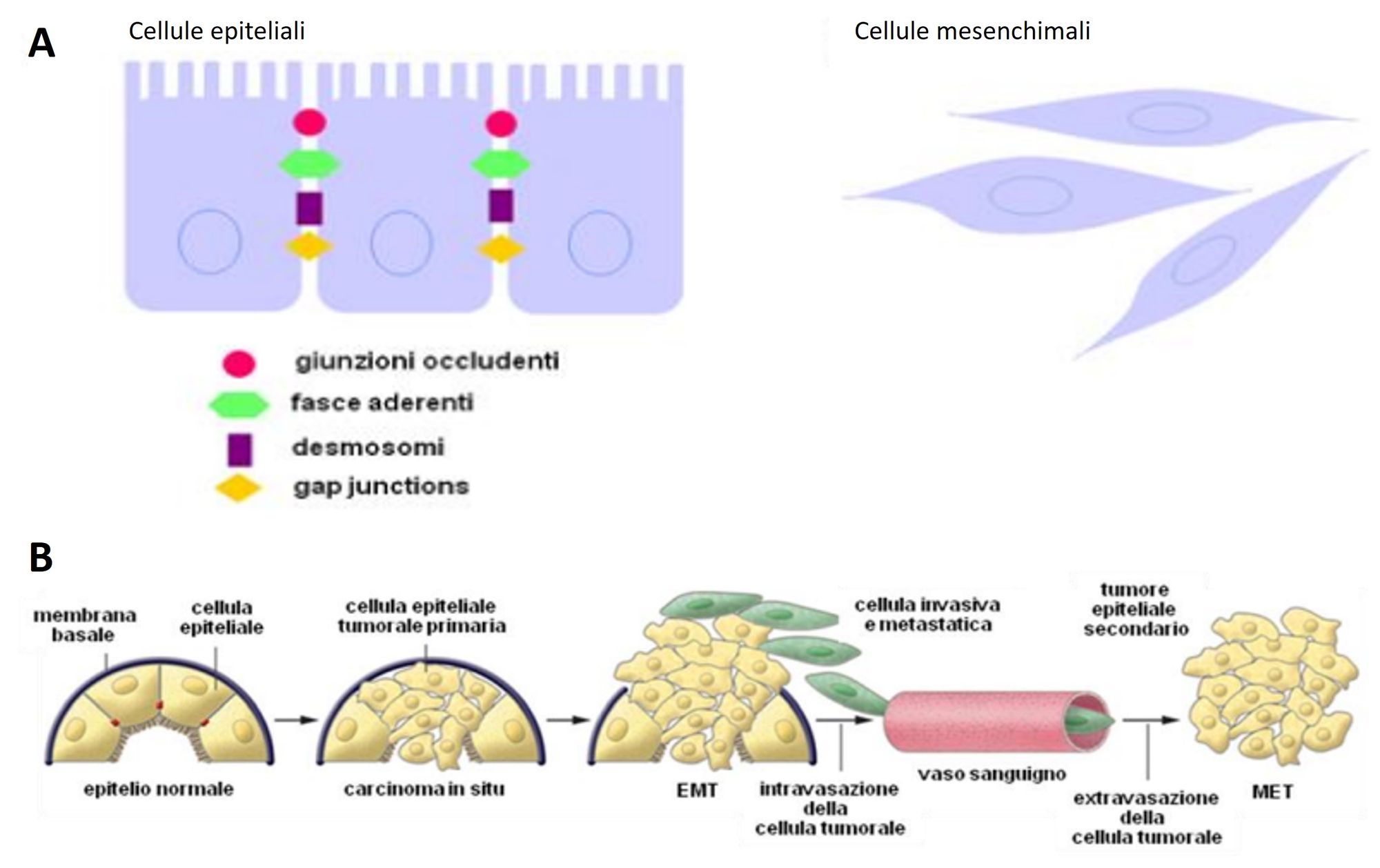
Nel carcinoma nasofaringeo, LMP-1 è implicata nella metastatizzazione e nell’invasività tramite l’attivazione di un fattore di trascrizione, Twist, che conduce alla transizione epitelio-mesenchimale (EMT) dei cheratinociti. Per EMT si intende un processo attraverso cui le cellule epiteliali, che hanno una forma simile a un quadrilatero, modificano la loro conformazione e assumono un aspetto più somigliante alle cellule mesenchimali, che sono fusiformi. In seguito a tale cambiamento, le cellule epiteliali perdono le proteine di membrana che assicurano l’adesione tra di esse (E-caderina, β-catenina, occludina), acquisiscono molecole mesenchimali (vimentina, fibronectina) e la capacità di migrare verso altri tessuti (Fig. 9).
Per quanto riguarda il linfoma di Burkitt, è interessante citare uno studio del 1999, pubblicato su Journal of Virology, che descrive dei fattori peculiari che contribuiscono al fenotipo maligno, ovvero gli EBERs (EBER1 e EBER2), che sono dei piccoli RNA non poliadenilati (privi della sequenza poliA) espressi dall’EBV. I ricercatori hanno constatato che tali RNA, se inseriti all’interno di cellule in coltura, favoriscono la proliferazione e la resistenza all’apoptosi.
Identificazione
Al fine di stabilire la presenza dell’HHV-4 in un individuo, esistono quattro metodi diagnostici:
- Ricerca dei linfociti atipici mediante analisi microscopica dello striscio di sangue;
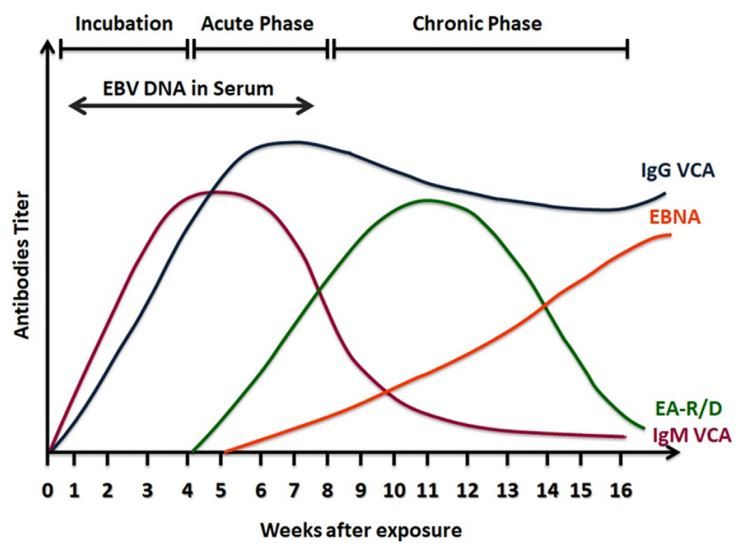
- Dosaggio degli anticorpi contro specifiche proteine virali tramite test ELISA (saggio immuno-assorbente legato a un enzima). Tra i vari anticorpi abbiamo gli anti-EBNA1, gli anti-MA (antigene di membrana), gli anti-EA (antigeni precoci) e gli anti-VCA (proteina del capside). A proposito di questi ultimi, è possibile rilevarne due tipologie, cioè IgM e IgG; i primi indicano un’infezione precoce, i secondi un’infezione pregressa. Bisogna evidenziare che mentre gli anticorpi anti-EA e le IgM anti-VCA scompaiono una volta terminata la fase acuta dell’infezione, gli anticorpi anti-EBNA1 e le IgG anti-VCA permangono per tutta la vita (Fig. 10);
- Saggio dell’avidità delle IgG anti-VCA, allo scopo di determinare lo stadio della patologia. Si tratta di un test ELISA modificato in cui viene aggiunta l’urea, una sostanza che rompe il legame tra anticorpi e antigeni, che è più forte nella fase tardiva e più debole in quella precoce;
- Analisi molecolari che individuano il DNA del virus e sono utili per quantificare la carica virale. Quello più utilizzato è la PCR (reazione a catena della DNA polimerasi), in cui si utilizzano oligonucleotidi che amplificato i seguenti geni: EBNA-1, EBNA-2, EBNA-3C, LMP-1, LMP-2 ed EBER1. È un metodo sensibile e affidabile, molto usato per monitorare lo stato immune di individui immunodepressi e per valutare il rischio potenziale di sviluppare malattie correlate all’EBV.
Terapia
Per la mononucleosi non esiste un trattamento specifico, bensì è opportuno rimanere a riposo durante la fase acuta, quando i sintomi sono più marcati; nel caso di splenomegalia, anche se i sintomi diminuiscono o scompaiono, è importante evitare, per almeno un mese, attività che possono provocare la rottura della milza, come il sollevamento pesi e gli sport di contatto. Per alleviare la febbre si possono usare antipiretici come paracetamolo, aspirina o ibuprofene, e se insorgono delle complicanze, come il gonfiore delle vie aeree, si può ricorrere ai corticosteroidi.
Passiamo alle patologie tumorali. Iniziando dal carcinoma nasofaringeo, considerato il sito in cui si forma, che tra l’altro abbonda di vasi e nervi, è difficile rimuoverlo con la chirurgia; quindi, la terapia si fonda soprattutto su chemioterapia, radioterapia e terapia mirata (con farmaci che contrastano i meccanismi specifici della carcinogenesi).
Il linfoma di Hodgkin può essere trattato tramite un ciclo chemioterapico con adriamicina, bleomicina, vinblastina e decarbazina, associato o no alla radioterapia, e l’immunoterapia. Quest’ultima, che è un tipo di terapia mirata, si basa sull’uso di anticorpi creati in laboratorio in grado di legarsi agli antigeni espressi dalle cellule tumorali e attivare la risposta immunitaria che le uccide; tra questi abbiamo Brentuximab, Pembrolizumab e Rituximab.
Per il linfoma di Burkitt si ricorre a chemioterapia intensiva alternata a base di vincristina, ciclofosfamide, doxurubicina, metotrexato, ifosfamide, etoposide e citarabina, associata all’anticorpo Rituximab.
Per quanto concerne i disordini linfoproliferativi post-trapianto, il trattamento prevede una riduzione della terapia immunosoppressiva, la somministrazione del Rituximab e l’immunoterapia cellulare; quest’ultima consiste nel prelevare dei linfociti da un donatore, espanderli in coltura mettendoli a contatto con uno specifico ceppo di EBV (B95-8), stimolarli con l’interleuchina 2, e iniettarli nel paziente. Tuttavia, questo metodo richiede un tempo cha va da uno a tre mesi.
EBV e sclerosi multipla
Da tempo l’infezione da EBV è considerata un fattore di rischio per l’insorgenza della sclerosi multipla, una malattia autoimmune e neurodegenerativa che coinvolge il sistema nervoso centrale (CNS) conducendo alla distruzione della mielina, una sostanza lipidica che riveste gli assoni e rende più veloce il passaggio dei segnali elettrochimici nel cervello. Le conseguenze della riduzione della mielina sono i disturbi visivi, i disturbi della sensibilità e la perdita progressiva del controllo muscolare. Ovviamente l’esistenza di una correlazione tra EBV e sclerosi multipla non significa che l’HHV-4 raffiguri la causa ufficiale della patologia e che coloro che entrano in contatto con il virus automaticamente la svilupperanno. Non dobbiamo dimenticare che le persone sieropositive nel mondo raggiungono il 90%, però solo una piccola frazione si ammala di sclerosi multipla, dal momento che ci sono ulteriori fattori che possono aumentare la probabilità, come la suscettibilità genetica, l’etnia e l’ambiente
Uno studio pubblicato su Science nel 2022 ha analizzato una coorte di più di 10 milioni di giovani adulti che avevano preso servizio nelle forze armate statunitensi dal 1993 al 2013, e 955 di questi erano stati colpiti dalla sclerosi multipla. I ricercatori raccolsero 801 campioni di siero prelevati ai militari in quel periodo e che erano conservati presso il Department of Defense Serum Repository (DoDSR); le analisi rivelarono che 35 erano inizialmente sieronegativi e 34 si erano infettati prima dell’esordio della malattia, mentre al momento della comparsa solo un campione su 801 era sieronegativo. Questi dati rafforzano la teoria secondo cui l’EBV è implicato nello sviluppo della sclerosi multipla.
Come è possibile che un virus che attacca i linfociti B inneschi una malattia nel CNS? Si è visto che nella sclerosi multipla i linfociti B e le plasmacellule esprimono un recettore particolare, l’integrina αV, che consente loro di superare la barriera ematoencefalica e raggiungere il cervello. In aggiunta a ciò, le plasmacellule presenti nel cervello vanno incontro a un’espansione clonale e producono anticorpi che vengono reperiti nel liquido cerebrospinale e bersagliano le cellule gliali che sintetizzano la mielina.
Comunque, il meccanismo attraverso cui l’EBV media lo sviluppo della sclerosi multipla rimane ambiguo. Una possibilità risiede nel fenomeno del mimetismo molecolare, ovvero le proteine virali che assumono caratteristiche strutturali simili a quelle della mielina e di altre proteine del CNS, deviando quindi la risposta immunitaria verso i tessuti dell’organismo. Un esempio è la proteina ANO2, un canale del cloro attivato dal calcio; in uno studio pubblicato su PNAS nel 2019, i ricercatori rimarcarono un incremento della concentrazione di anticorpi anti-ANO2 nella sclerosi multipla e che questi anticorpi riconoscevano anche un frammento della proteina virale EBNA-1. In questa maniera la risposta immunitaria verso il virus può promuovere l’infiammazione del CNS, probabilmente tramite i linfociti T. Un ulteriore esempio riguarda la rilevazione di anticorpi aventi un’affinità per EBNA-1 e per la proteina GlialCAM (una proteina importante per l’adesione e il movimento cellulare) in pazienti affetti da sclerosi multipla, ingaggiati in un lavoro pubblicato su Nature nel 2022.
Detto questo, l’infezione da EBV è probabilmente necessaria però non è sufficiente a provocare la malattia. Oltre ai fattori che alzano il rischio di insorgenza, elementi aggiuntivi dovranno essere messi in luce per chiarirne appieno la fisiopatologia.
Lorenzo Tramontana
Fonti
- https://www.issalute.it/index.php/la-salute-dalla-a-alla-z-menu/v/virus-di-epstein-barr-epv
- https://www.ncbi.nlm.nih.gov/books/NBK304353/
- Maria K. Smatti, Duaa W. Al-Sadeq, Nadima H. Ali, Gianfranco Pintus, Haissam Abou-Saleh and Gheyath K. Nasrallah. 2018. “Epstein–Barr Virus Epidemiology, Serology, and Genetic Variability of LMP-1 Oncogene Among Healthy Population: An Update”, Frontiers in Oncology
- Luciana Cristina Fagundes Gequelin, Irina N. Riediger, Sueli M. Nakatani, Alexander W. Biondo and Carmem M. Bonfim. 2011. “Epstein-Barr virus: general factors, virus-related diseases and measurement of viral load after transplant”, Rev Bras Hematol Hemoter
- Yao Chang, Che-Huang Tung, Yu-Tzu Huang, Jean Lu, Jen-Yang Chen, and Ching-Hwa Tsai. 1999. “Requirement for Cell-to-Cell Contact in Epstein-Barr Virus Infection of Nasopharyngeal Carcinoma Cells and Keratinocytes”, Journal of Virology
- Paul J. Farrell. “2002. Cell-switching and kissing”, Nature Medicine
- Hua Zhang, Yan Li, Hong-Bo Wang, Ao Zhang, Mei-Ling Chen, Zhi-Xin Fang, Xiao-Dong Dong, Shi-Bing Li, Yong Du, Dan Xiong, Jiang-Yi He, Man-Zhi Li, Yan-Min Liu, Ai-Jun Zhou, Qian Zhong, Yi-Xin Zeng, Elliott Kieff, Zhiqiang Zhang , Benjamin E. Gewurz, Bo Zhao and Mu-Sheng Zeng. 2017 “Ephrin receptor A2 is an epithelial cell receptor for Epstein–Barr virus entry”, Nature Microbiology
- Matteo Riccò. 2005. “Il morbo di Hodgkin malattia professionale del personale agricolo?”, Researchgate
- Wanla Kulwichit, Rachel Hood Edwards, Ethan M. Davenport, John F. Baskar, Virginia Godfrey, and Nancy Raab-Traub. 1998. “Expression of the Epstein–Barr virus latent membrane protein 1 induces B cell lymphoma in transgenic mice”, PNAS
- Robert G Caldwell, Joanna B Wilson, Steven J Anderson, Richard Longnecker. 1998. “Epstein-Barr Virus LMP2A Drives B Cell Development and Survival in the Absence of Normal B Cell Receptor Signals”, Immunity
- Toshiyuki Horikawa, Jing Yang, Satoru Kondo, Tomokazu Yoshizaki, Irene Joab, Mitsuru Furukawa and Joseph S. Pagano. 2007. “Twist and Epithelial-Mesenchymal Transition Are Induced by the EBV Oncoprotein Latent Membrane Protein 1 and Are Associated with Metastatic Nasopharyngeal Carcinoma”, Cancer Research
- Jun Komano, Seiji Maruo, Koichi Kurozumi, Takanori Oda and Kenzo Takada. 1999. “Oncogenic Role of Epstein-Barr Virus-Encoded RNAs in Burkitt’s Lymphoma Cell Line Akata”, Journal of Virology
- William H. Robinson and Lawrence Steinman. 2022. “Epstein-Barr virus and multiple sclerosis”, Science
- Katarina Tengvalla, Jesse Huanga, Cecilia Hellströmc, Patrick Kammerd, Martin Biströme, Burcu Ayogluf, Izaura Lima Bomfima,b, Pernilla Stridha, Julia Buttd, Nicole Brennerd, Angelika Micheld, Karin Lundbergb, Leonid Padyukovb, Ingrid E. Lundbergb, Elisabet Svenungssong, Ingemar Ernbergh, Sigurgeir Olafssoni, Alexander T. Diltheyj, Jan Hillerta, Lars Alfredssonl, Peter Sundströme, Peter Nilssonc, Tim Waterboerd, Tomas Olssona, and Ingrid Kockum. 2019. “Molecular mimicry between Anoctamin 2 and Epstein-Barr virus nuclear antigen 1 associates with multiple sclerosis risk”, PNAS
- Tobias V. Lanz, R. Camille Brewer, Peggy P. Ho, Jae-Seung Moon, Kevin M. Jude, Daniel Fernandez, Ricardo A. Fernandes, Alejandro M. Gomez, Gabriel-Stefan Nadj, Christopher M. Bartley, Ryan D. Schubert, Isobel A. Hawes, Sara E. Vazquez, Manasi Iyer, J. Bradley Zuchero, Bianca Teegen, Jeffrey E. Dunn, Christopher B. Lock, Lucas B. Kipp, Victoria C. Cotham, Beatrix M. Ueberheide, Blake T. Aftab, Mark S. Anderson, Joseph L. DeRisi, Michael R. Wilson, Rachael J.M. Bashford-Rogers, Michael Platten, K. Christopher Garcia, Lawrence Steinman, William H. Robinson. 2022. “Clonally Expanded B Cells in Multiple Sclerosis Bind EBV EBNA1 and GlialCAM”, Nature
- Catherine M. Bollard, Cliona M. Rooney & Helen E. Heslop. 2012. “T-cell therapy in the treatment of post-transplant lymphoproliferative disease”, Nature Reviews of Clinical Oncology
- Paolo Corradini e Robin Foà. 2015. “Manuale di Ematologia. II edizione”, Edizione Minerva Medica
- https://www.creative-diagnostics.com/tag-epstein-barr-virus-antigens-15.htm
- https://www.sciencephoto.com/media/248221/view/tem-of-epstein-barr-virus
- https://www.msdmanuals.com/it-it/casa/infezioni/infezioni-da-herpesvirus/mononucleosi-infettiva
- https://www.orpha.net/consor/cgi-bin/OC_Exp.php?Lng=IT&Expert=150
- https://www.msdmanuals.com/it-it/professionale/ematologia-e-oncologia/linfomi/linfoma-di-burkitt
- https://www.msdmanuals.com/it-it/professionale/ematologia-e-oncologia/linfomi/linfoma-di-hodgkin
- https://www.thelancet.com/journals/lancet/article/PIIS0140-6736%2819%2932962-9/fulltext
- https://www.leukemia-cell.org/atlas/index.php?pg=images--mature-b-cell-neoplasms--burkitt-lymphoma#1
- https://medicinalive.com/linfoma-di-burkitt/
- https://air.unimi.it/retrieve/dfa8b991-a068-748b-e053-3a05fe0a3a96/phd_unimi_R09599.pdf
- https://www.airc.it/cancro/informazioni-tumori/guida-ai-tumori/linfoma-di-hodgkin
Ti è piaciuto l'articolo?
 BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
