Batteri mangia-carne: facciamo luce sulla Fascite Necrotizzante
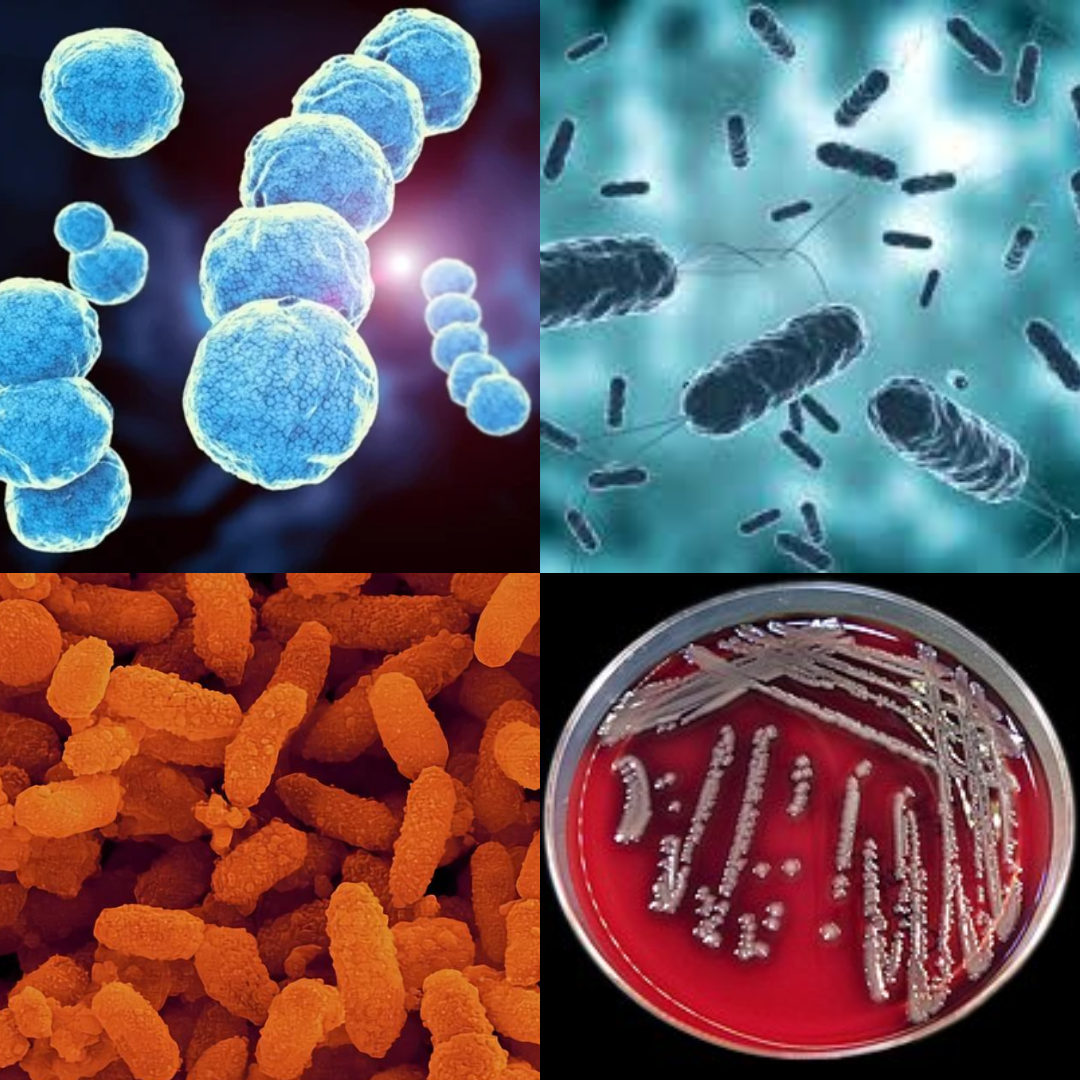
L’espressione “batteri mangia-carne” indica un gruppo di microbi responsabili di una patologia letale chiamata fascite necrotizzante; il termine non è proprio adatto, dal momento che questi microorganismi non consumano i tessuti, bensì rilasciano delle molecole proteiche particolari che determinano infiammazione e necrosi (morte cellulare) delle fasce, ovvero i rivestimenti sottocutanei che circondano i tessuti muscolare e adiposo, i nervi e i vasi sanguigni.
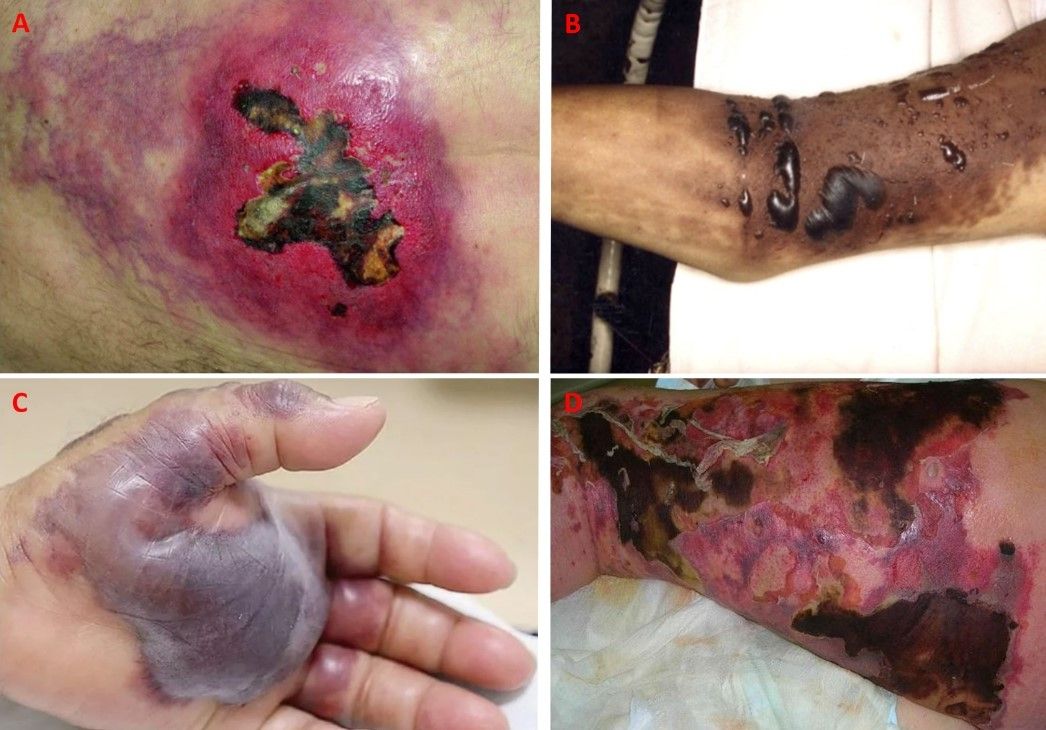
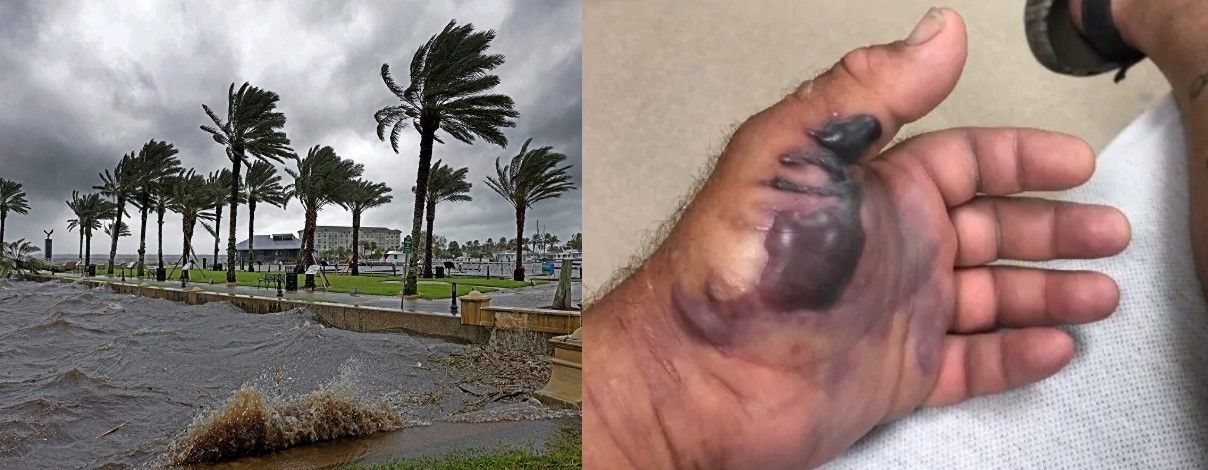
La fascite necrotizzante colpisce 3,5 persone su 100000, si sviluppa soprattutto negli arti inferiori, anche se può coinvolgere anche la parete addominale e il perineo (gangrena di Fournier), e sopraggiunge nel momento in cui i batteri, entrando da lesioni di diversi tipi come tagli, abrasioni, ferite chirurgiche, ferite da siringhe, ustioni e punture di insetti, raggiungono i tessuti più profondi attraverso il flusso ematico. La malattia si manifesta in questo modo: all’inizio compaiono cellulite, eritema e gonfiore che si espandono, tumefazione, dolore e febbre, dipoi la pelle cambia colore diventando bluastra o violacea, e ciò è legato alla trombosi dei piccoli vasi sanguigni nelle papille dermiche (Fig. 1). La trombosi comporta l’occlusione dei vasi, con conseguente ischemia tissutale, infarto e necrosi cutanea. Al contempo si formano macchie nere, vesciche e ulcere, si ha fuoriuscita di siero o pus dalle zone infette, i tessuti necrotizzati sprigionano un odore di decomposizione, e i pazienti accusano vertigini, stanchezza, diarrea e nausea. In assenza di un trattamento idoneo e tempestivo, la patologia conduce a perdita degli arti, sepsi, insufficienza multiorgano e shock, fino ad arrivare alla morte.
Esistono molteplici fattori che incrementano il rischio di insorgenza della malattia, ovvero fratture esposte, da cui i batteri possono penetrare, vasculopatia periferica, diabete, indebolimento del sistema immunitario dovuto a cirrosi epatica, farmaci immunosoppressivi, tumori e malattie renali, e abuso di farmaci antinfiammatori. In casi rari può insorgere nei neonati affetti da onfalite (infiammazione dell’ombelico).
Adesso faremo una breve descrizione dei batteri raffiguranti gli agenti patogeni della fascite necrotizzante, focalizzandoci su Streptococcus pyogenes, Vibrio vulnificus e Aeromonas hydrophila.
Streptococcus pyogenes
S. pyogenes è un batterio Gram positivo, immobile, aerobio-anaerobio facoltativo, dotato di capsula, catalasi e ossidasi negativo, asporigeno e beta-emolitico; nella classificazione di Lancefield, che si basa sui polisaccaridi di superficie, appartiene agli streptococchi di gruppo A. Raffigura un microorganismo commensale che risiede nelle vie aeree superiori, quindi naso-faringe e tonsille, dove in alcune circostanze provoca infiammazioni acute come faringo-tonsillite. In aggiunta a ciò, è responsabile anche di altre malattie, tra cui impetigine, erisipela, scarlattina, cellulite, febbre reumatica e glomerulonefrite acuta.
Dal punto di vista filogenetico, appartiene al phylum Firmicutes, alla classe dei Cocchi, all’ordine Lactobacillales e alla famiglia Streptococcaceae.
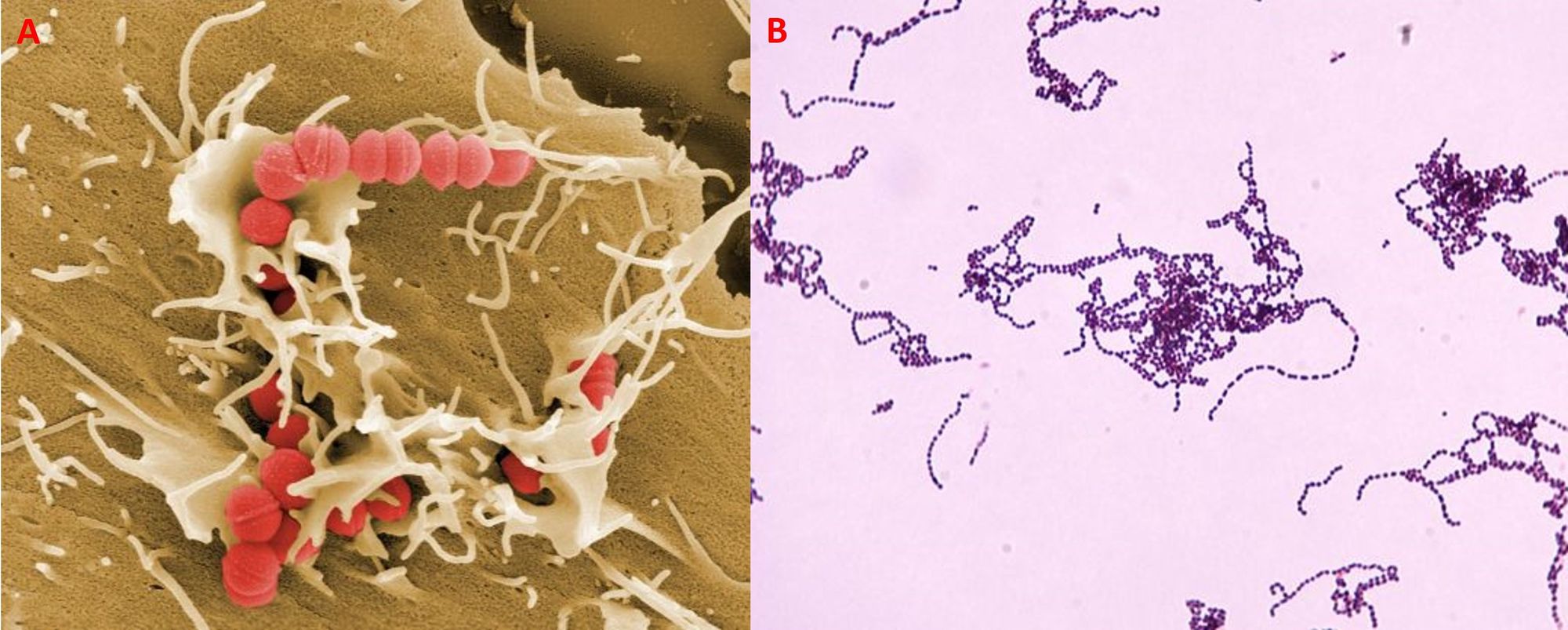
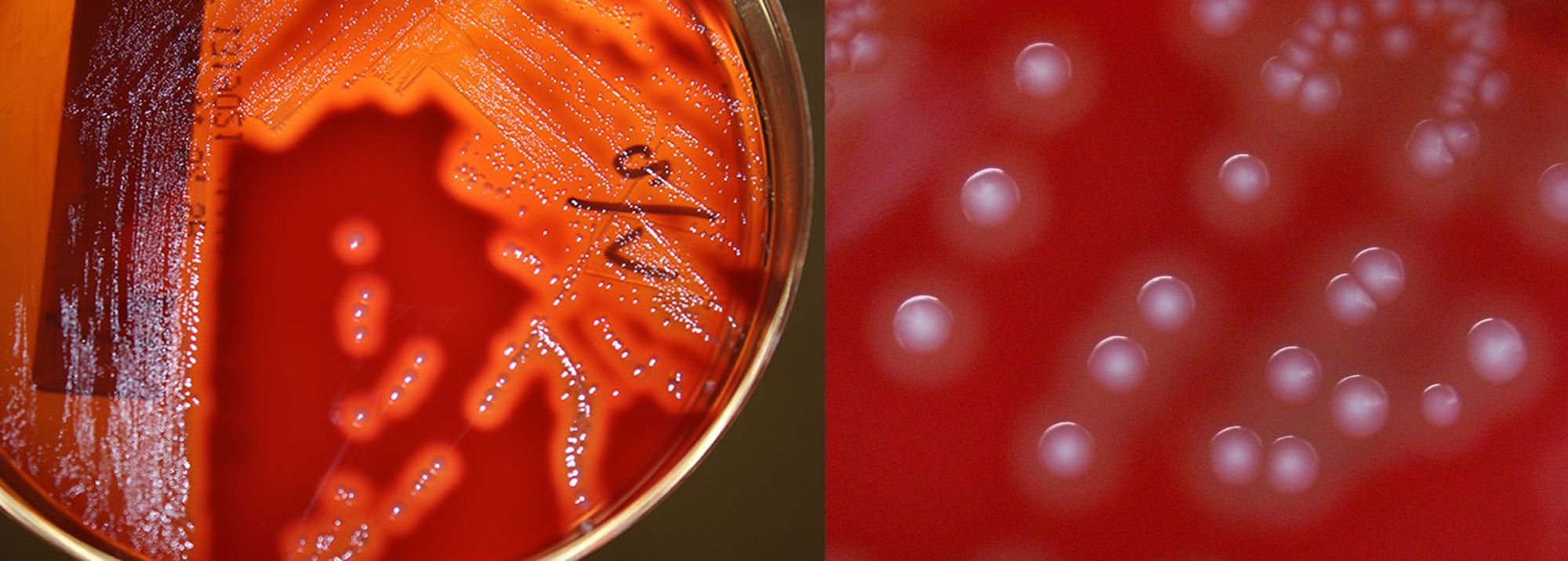
A livello microscopico presenta una forma sferoidale od ovoidale e si dispone a catenelle (Fig. 2), mentre dal punto di vista macroscopico su agar sangue crea delle colonie bianco-grigiastre, di 1-2 mm di diametro, a forma di cupola, dalla superficie liscia e i margini netti, circondate da un alone di beta-emolisi (Fig. 3), ovvero il germe induce una lisi completa dei globuli rossi presenti nel terreno di coltura.
Fattori di virulenza di S. pyogenes:
- La capsula, che impedisce la fagocitosi da parte dei macrofagi e dei granulociti neutrofili;
- La proteina M, la proteina F e l’acido lipoteicoico, che agiscono come delle adesine, cioè permettono l’adesione del batterio, e promuovono l’entrata nella cellula ospite;
- La streptolisina O e la streptolisina S, due tossine che lisano i leucociti, gli eritrociti e le piastrine;
- Quattro enzimi, ognuno con una funzione diversa: la streptochinasi, che scioglie i coaguli di fibrina, la ialuronidasi, che consente l’invasione dei tessuti, la DNAsi, che depolimerizza il DNA rilasciato dai neutrofili morenti che formano il pus, e la C5a peptidasi, che degrada la proteina C5a, un componente del sistema del complemento che richiama i globuli bianchi nella zona dell’infiammazione;
- Le tossine pirogeniche (SPE-A, SPE-B, SPE-C, SPE-F), chiamate anche superantigeni, che causano l’insorgenza di varie malattie, tra cui la fascite necrotizzante, la sepsi e la scarlattina. Queste molecole attivano una grossa mole di linfociti T, con conseguente elevata secrezione di citochine, attivazione del complemento e della via della coagulazione, e produzione di radicali liberi; a giocare questi ruoli sono i linfociti T CD4 e le citochine TNF-α e TNF-β (fattore di necrosi tumorale alfa e beta).
Vibrio vulnificus
V. vulnificus è un bacillo Gram negativo, mobile, anaerobio facoltativo, catalasi e ossidasi positivo, asporigeno e alofilo (predilige gli ambienti ad alta salinità); ne esistono due forme, ossia virulenta e avirulenta, che vuol dire rispettivamente dotata e priva di capsula. Questo batterio risiede in ambienti acquatici come fiumi, estuari, delta e battigie, come anche sul fondale oceanico, ed entra nella catena alimentare contaminando lo stomaco delle ostriche, che sono i portatori primari, ma anche di altri molluschi come vongole, cozze e capesante. Occasionalmente può ritrovarsi nell'intestino dei pesci.
L’infezione umana avviene quando si ingeriscono o si manipolano molluschi crudi infetti o acqua contenente il batterio; nel primo caso si ha gastroenterite con febbre, brividi, diarrea acquosa, nausea e vomito, mentre nel secondo caso compare cellulite con presenza di bolle che, se non trattata, evolve in fascite necrotizzante.
Filogeneticamente V. vulnificus rientra nel phylum Proteobacteria, nella classe Gamma Proteobacteria, nell’ordine Vibrionales e nella famiglia Vibrionaceae. Gran parte dei batteri appartenenti a questa famiglia si trovano nei mari più caldi (tra 9° e 31° C) e proliferano specialmente nelle zone subtropicali con clima monsonico. Non a caso il riscaldamento globale è correlato con l’aumento della prevalenza e della virulenza di questi microorganismi.
Dal punto di vista morfologico, V. vulnificus ha una forma bastoncellare con una lieve curvatura ed è dotato di un flagello, su agar sangue forma delle colonie di 3 mm, bianco-grigiastre e lucide (alcuni ceppi creano emolisi), mentre su TCBS (Thiosulfate Citrate Bile Sucrose) agar, il più usato per l'identificazione, le colonie sono verdi-blu.
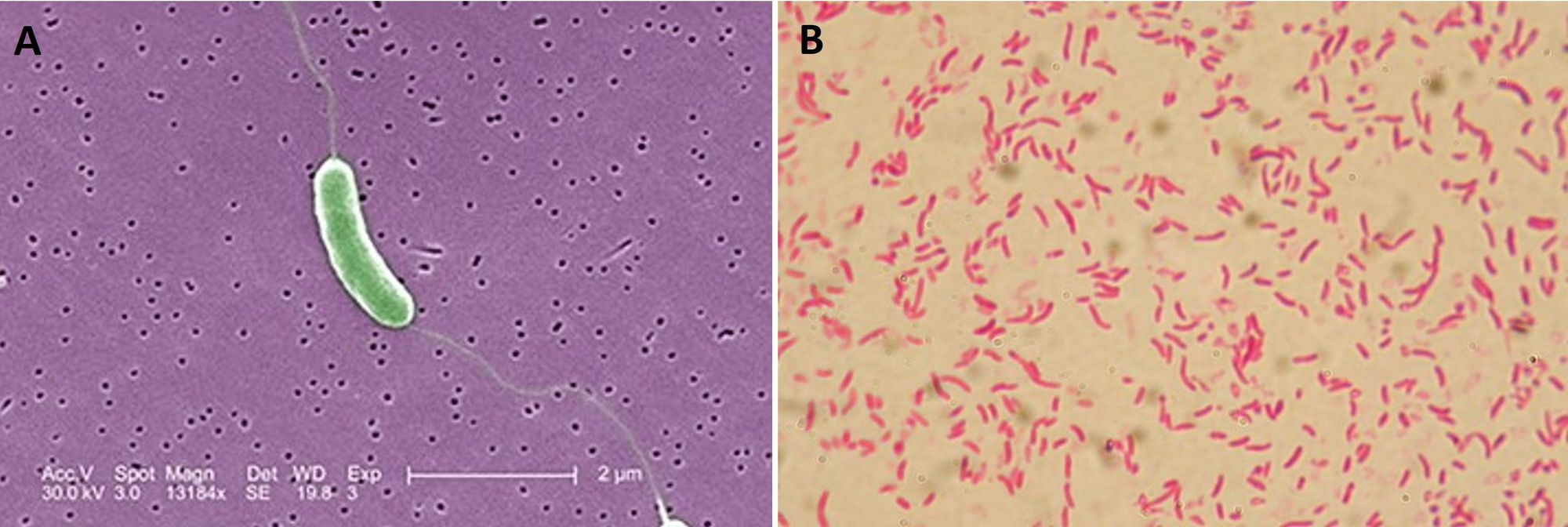
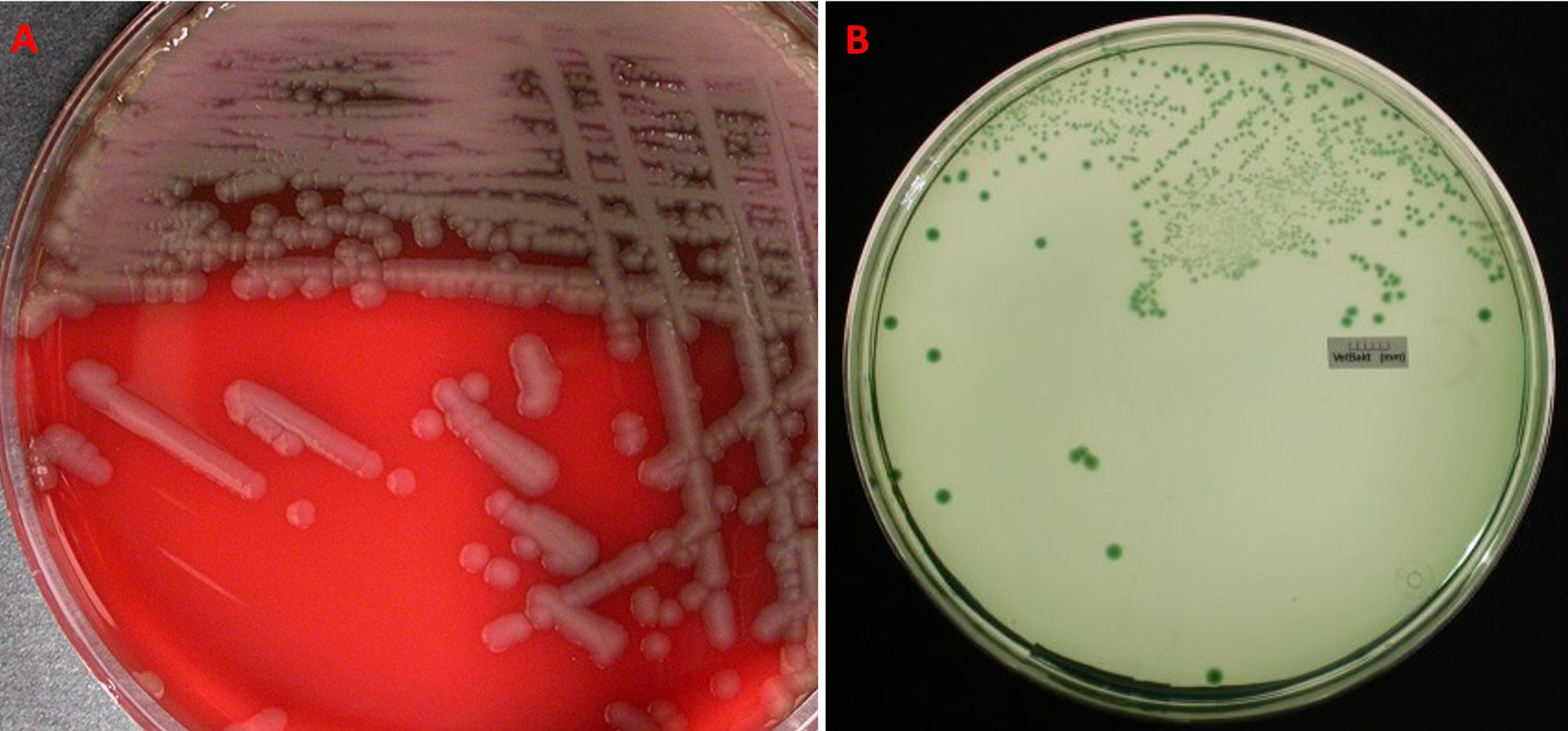
V. vulnificus possiede i seguenti fattori di virulenza:
- La capsula, che lo rende virulento;
- Il lipopolisaccaride, che rappresenta la parte principale della membrana esterna ed è costituito da tre componenti, ovvero l’antigene O, il core e il lipide A. Quest’ultimo è il fattore di virulenza vero e proprio che si libera con la rottura della cellula e stimola la produzione massiva di TNF-α concorrendo alla setticemia;
- Gli enzimi collegenasi, elastasi, lipasi e DNAsi; eccetto il quarto, gli altri tre demoliscono i tessuti connettivi affinché il batterio ci si possa infiltrare;
- L’elastolitica, una proteina che stimola la vasodilatazione, la contrattilità della muscolatura liscia, aumenta la permeabilità vascolare e contribuisce all’espansione del batterio nel circolo ematico consentendo la setticemia.
Aeromonas hydrophila
A. hydrophila è un bacillo Gram negativo, capsulato, asporigeno, mobile mediante un flagello polare, anaerobio facoltativo, catalasi e ossidasi positivo. È frequente nelle regioni temperate e risiede in molteplici ambienti, ossia nei mari, nei fiumi, nei torrenti, nel suolo, nelle piscine, nelle acque dei rubinetti e negli scarichi fognari. È in grado di sopravvivere a temperature inferiori a 4° C e prolifera bene a 28° C. Nonostante sia prevalentemente un patogeno di pesci e anfibi, può provocare malattie anche in altri organismi come rettili, chiocciole, bovini ed esseri umani. In questi ultimi, in seguito a ingestione e/o manipolazione di acqua contaminata e pesce crudo infetto, provoca gastroenteriti (un tipo con diarrea e sintomi analoghi al colera e un altro con dissenteria), sepsi e infezioni di ferite che possono evolvere in fascite necrotizzante. Poiché nei pazienti immunodepressi determina l’insorgenza di infezioni ad elevata mortalità, è considerato un batterio opportunista.
Al livello filogenetico è incluso nel phylum Proteobacteria, nella classe Gamma Proteobacteria, nell’ordine Aeromonadales e nella famiglia Aeromonadaceae.
Microscopicamente A. hydrophila è caratterizzato da una forma bastoncellare diritta o ricurva (Fig. 6), mentre macroscopicamente genera delle colonie tonde, lisce, convesse e con un colore dissimile in base al terreno: su Tryptic Soy agar (TSA) sono bianco-giallastre, opache e semi-traslucide, su TCBS agar presentano un colore giallo acceso grazie alla fermentazione del saccarosio (tale processo acidifica il terreno con conseguente viraggio al giallo del blu di bromotimolo, che è l’indicatore di pH), e su agar sangue sono grigio-verdastre o bianche, accerchiate da un alone di beta-emolisi (Fig. 7).
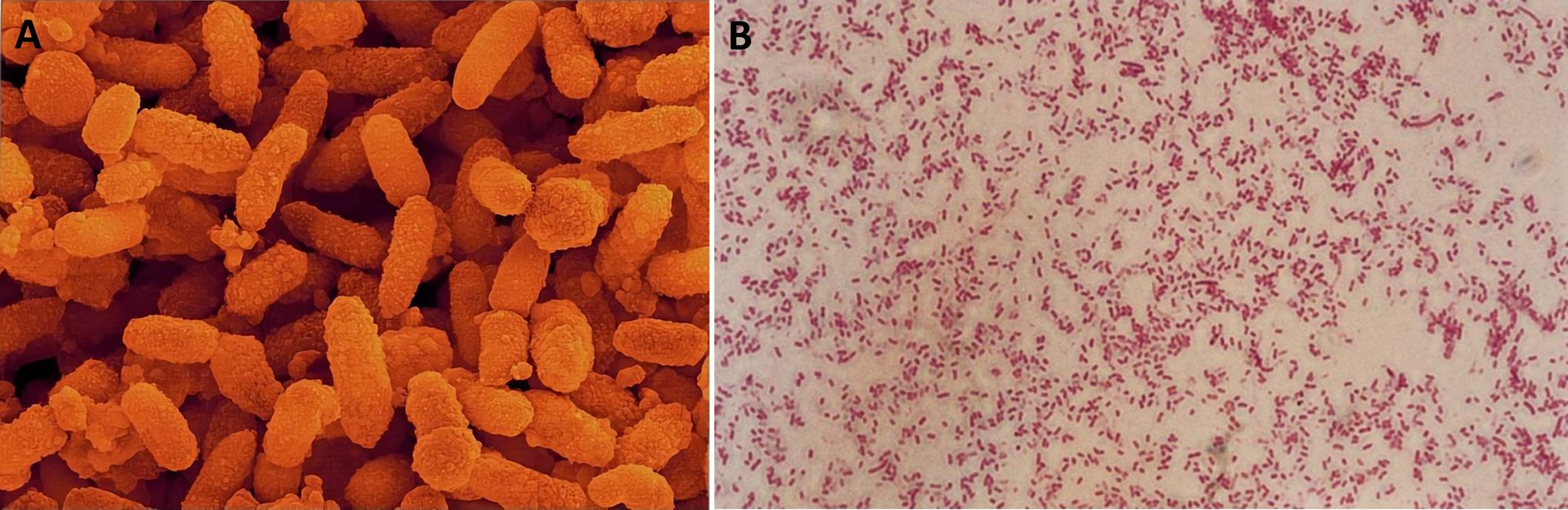
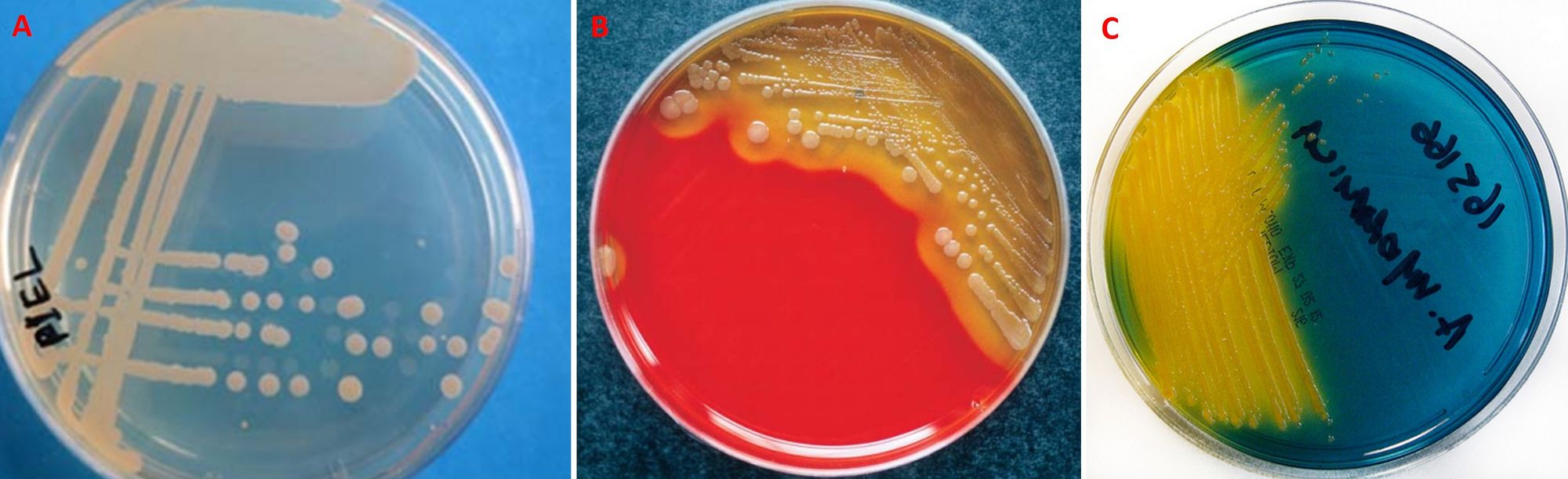
Elenchiamo ora il considerevole numero di fattori di virulenza di A. hydrophila:
- La capsula;
- Il sistema di secrezione di tipo 2 (T2SS), che promuove la liberazione extracellulare di un ampio range di fattori di virulenza, in cui sono incluse l’aerolisina (una tossina citotossica), le amilasi, le DNasi e le proteasi;
- Il sistema di secrezione di tipo 3 (T3SS), che inietta delle tossine nelle cellule. Uno degli effettori appartenenti a questo sistema è AexU, che stimola la morte cellulare programmata (apoptosi) attivando la caspasi 3, altera varie funzioni cellulari necessarie all’annientamento dei patogeni (come la chemiotassi e la fagocitosi) distruggendo il citoscheletro di actina, ostacola la via di segnalazione di NF-kB (nuclear factor kappa-light-chain-enhancer of activated B cells) con conseguente diminuzione della secrezione di citochine pro-infiammatorie come l’interleuchina 6, l’interleuchina 8 e l’interleuchina 1β. Inoltre, questa molecola causa l’infiammazione nell’interstizio polmonare, la necrosi alla milza e al fegato;
- Il sistema di secrezione di tipo 6 (T6SS), che, in maniera simile al precedente, inocula nelle cellule dei fattori di virulenza. Ciò avviene tramite una proteina G con sequenze ripetute di valina e glicina (VrgG) e una proteina co-regolata dall’emolisina (Hcp); quest’ultima forma dei pori sulla membrana plasmatica;
- Gli antigeni O della membrana, che agevolano la colonizzazione;
- La genesi del biofilm, un substrato mucopolisaccaridico che consente ai batteri di incollarsi alle superfici e proteggersi da agenti antimicrobici e dal sistema immunitario dell’ospite;
- Le emolisine, che sono delle proteine che contribuiscono alla disintegrazione diretta o indiretta delle cellule mediante lisi. La più abbondante è l’emolisina extracellulare termolabile (Ahh1), che possiede il maggiore potere citotossico quando agisce in sinergia con l’aerolisina A (AerA);
- Enzimi degradativi come la collagenasi, l’elastasi, le lipasi, le metalloproteasi, le serina proteasi e l’enolasi. Questi cooperano alla virulenza, dal momento che consentono al batterio di distruggere i tessuti connettivi e aumentare l’invasività.
È importante rimarcare una caratteristica particolare di A. hydrophila a proposito dell’innesco della fascite necrotizzante: l’infezione si verifica solo se sono presenti due ceppi, cioè NF2 e NF1. Il primo sintetizza l’esotossina A (ExoA), attraverso cui il batterio attraversa il tessuto muscolare e penetra nel torrente ematico, mentre il secondo sfrutta il meccanismo di NF2 per arrivare nel circolo sanguigno, e rilascia l’effettore TseC del sistema di secrezione di tipo 6 (TSS6), che uccide NF2.
Diagnosi
La fascite necrotizzante prevede un approccio diagnostico basato su diverse procedure che sono necessarie al fine di valutare lo stato dell’organismo e la crescita batterica:
- Anamnesi ed esame obiettivo;
- Conta dei leucociti e dosaggio della proteina C reattiva (PCR), che nella fascite necrotizzante sono alti;
- Emocoltura;
- Indagine microscopica e colturale di tamponi da ferite e dell’essudato;
- Esecuzione di una biopsia;
- Tomografia computerizzata e risonanza magnetica.
È fondamentale effettuare una diagnosi differenziale, dal momento che la fascite necrotizzante esibisce delle proprietà simili ad altre patologie come la cellulite di grado severo e la gangrena gassosa.
Terapia e profilassi
Innanzitutto, dato che la fascite necrotizzante è fatale, il paziente deve essere ricoverato in ospedale, spesso nei reparti di terapia intensiva. Il trattamento si fonda sulla somministrazione intravenosa di una mistura di antibiotici, allo scopo di incrementare lo spettro d’azione (alcuni di questi sono gentamicina, ampicillina, metronidazolo, imipenem, meropenem); in aggiunta a ciò, bisogna effettuare la rimozione chirurgica dei tessuti necrotici mediante il metodo dello sbrigliamento, eventualmente seguito dalla ricostruzione. Tale procedura è essenziale perché in seguito alla distruzione tissutale da parte dei batteri, il flusso ematico è ridotto, quindi i farmaci non raggiungono tutte le aree infette. Se l’infezione diventa incontrollabile, si ricorre all’amputazione dell’arto, e nei casi più gravi è necessaria la trasfusione. Dopo la rimozione si applica un bandeggio sterile e, nei giorni successivi, è opportuno controllare la potenziale presenza di ulteriori tessuti infetti, che vanno rimossi.
A fine intervento, sono previsti vari giorni di degenza, al fine di assicurarsi l’assenza di focolai di infezione, controlli delle medicazioni quotidiane e misurazione costante di vari parametri vitali come la pressione ematica, la frequenza cardiaca, la temperatura corporea e la saturazione sanguigna.
A proposito della profilassi, non esistono vaccini contro i batteri sopra descritti, dunque le strategie migliori prevedono la disinfezione corretta delle ferite, l’uso di guanti protettivi quando si manipolano molluschi e pesci crudi, e acqua che potrebbe essere contaminata.
Fonti
- https://www.msdmanuals.com/it-it/professionale/disturbi-dermatologici/infezioni-batteriche-cutanee/infezione-necrotizzante-dei-tessuti-molli
- https://www.infectiousdiseaseadvisor.com/home/decision-support-in-medicine/infectious-diseases/cellulitis-necrotizing-fasciitis-subcutaneous-tissue-infections/
- https://www.cdc.gov/groupastrep/diseases-hcp/necrotizing-fasciitis.html#r3
- https://healthy.thewom.it/salute/fascite-necrotizzante/
- https://www.unife.it/medicina/lm.odontoiatria/insegnamenti/scienze-mediche-i/modulo-di-microbiologia-clinica/aa-2015-16/4-Malattie%20da%20Streptococchi
- http://textbookofbacteriology.net/streptococcus_2.html
- Barbara Spellerberg and Claudia Brandt. 2016. “Laboratory Diagnosis of Streptococcus pyogenes (group A streptococci)”, Streptococcus pyogenes: Basic Biology to Clinical Manifestations
- J. M. Young. 1994. “Necrotising fasciitis”, The Lancet
- Se Young Park, Hyun Min Nam, Kun Park, Seok Don Park. 2011. “Aeromonas hydrophila Sepsis Mimicking Vibrio vulnificus Infection”, Ann Dermatol
- https://blogs.bcm.edu/2022/02/24/from-the-labs-novel-strategy-improved-sepsis-outcomes-in-animal-model/
- https://www.infectiousdiseaseadvisor.com/home/decision-support-in-medicine/infectious-diseases/streptocococcus-pyogenes/
- http://www.bacteriainphotos.com /Streptococcus%20pyogenes.html
- https://www.psoriasimetodoapollo.com/guida-alla-psoriasi-guttata/
- https://www.notizie.it/batteri-mangiacarne-in-florida-dopo-l-uragano-ian-almeno-4-morti-e-29-contagi/?refresh_ce
- https://www.uncome.it/salute/articolo/come-si-contrae-la-fascite-necrotizzante-19455.html
- https://www.ncbi.nlm.nih.gov/books/NBK554404/
- https://www.vetbact.org/species/84#
- https://www.cell.com/trends/microbiology/fulltext/S0966-842X%2819%2930219-7
- https://microbe-canvas.com/Bacteria/gram-negative-rods/facultative-anaerobic-3/catalase-positive-3/oxidase-positive/indole-positive-3/vibrio-vulnificus.html
- Melissa K. Jones and James D. Oliver. 2009. “Vibrio vulnificus: Disease and Pathogenesis”, Infection and Immunity
- Sing-Peng Heng, Vengadesh Letchumanan, Chuan-Yan Deng, Nurul-Syakima Ab Mutalib, Tahir M. Khan, Lay-Hong Chuah, Kok-Gan Chan, Bey-Hing Goh, Priyia Pusparajah and Learn-Han Lee. 2017. “Vibrio vulnificus: An Environmental and Clinical Burden”, Frontiers in Microbiology
- Shamsun Nahar, Mohammad Mizanur Rahman, Gias Uddin Ahmed and
Md. Ali Reza Faruk. 2016. “Isolation, identification, and characterization of Aeromonas hydrophila from juvenile farmed pangasius (Pangasianodon hypophthalmus)”, International Journal of Fisheries and Acquatic Studies - Irena Zdovc, Tanja Švara, Polona Juntes, Tina Kotnik, Matjaž Ocepek, Manica Černe, Milan Pogačnik. 2004. “The role of Aeromonas hydrophila bacterium as a causative agent of septicaemia in dogs”, Slov Vet Res
- https://www.sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/aeromonas-hydrophila
- https://www.medical-labs.net/aeromonas-bacteria-2440/
- https://www.creative-biolabs.com/vaccine/aeromonas-hydrophila-vaccines.htm
- https://www.alimenti-salute.it/content/enterite-aeromonas
- http://www.antimicrobe.org/b74.asp
- Johanna C. Sierra, Giovanni Suarez, Jian Sha,Wallace B. Baze, Sheri M. Foltz and Ashok K. Chopra. 2010. “Unraveling the mechanism of action of a new type III secretion system effector AexU from Aeromonas hydrophila”, Microbial Pathogenesis
- Fernández-Bravo, Paul B. Kilgore, Jourdan A. Andersson, Elizabeth Blears, Maria José Figueras, Nur A. Hasan, Rita R. Colwell, Jian Sha, and Ashok K. Chopra. 2019. “T6SS and ExoA of flesh-eating Aeromonas hydrophila in peritonitis and necrotizing fasciitis during mono-and polymicrobial infections”, Proceedings of the National Academy of Sciences
Ti è piaciuto l'articolo?
 BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
